Gene zum Schweigen bringen
Die sogenannte Ribonukleinsäure-(RNA-)Interferenz ist eine relativ neue Methode. Sie unterbindet, dass der Körper ein bestimmtes Protein bildet. Dies könnte Patienten bei verschiedenen Erkrankungen künftig helfen. Bei Sanofi am Standort Frankfurt setzen Forscherteams diese Methode seit einigen Jahren ein.
Um zu verhindern, dass der Körper ein bestimmtes, schädigendes Protein bildet, muss die dazugehörige Boten-RNA ausgeschaltet werden. Dies gelingt, indem sogenannte „small interferring RNA (siRNA)“ – kurze, einzel- oder doppelsträngige Ribonukleinsäure-Moleküle – in die Zelle geschleust wird. Dort bindet die siRNA an die Boten-RNA und zerstört diese: Der Körper kann das entsprechende Protein nicht mehr herstellen.
In einigen klinischen Studien wird diese Methode bereits eingesetzt. Unter anderem in der Erforschung von Therapien bei seltenen Bluterkrankungen oder Erkrankungen wie der „Transthyretin-assoziierte familiäre Amyloid-Polyneuropathie“. Bei dieser vererbbaren Krankheit bilden veränderte Proteine Strukturen aus, die sich im Nervensystem, aber auch in Herz, Niere oder Verdauungssystem ablagern. Ein auf der Ribonukleinsäure-Interferenz Methode basierender Wirkstoff wurde kürzlich von der amerikanischen Arzneimittelbehörde FDA zugelassen.
Am Ursprungsorgan ansetzen
Sanofi legt den Schwerpunkt der Forschung in diesem Bereich nicht nur auf Seltene Erkrankungen. Die Forschungsansätze fokussieren sich unabhängig davon auch auf Krankheiten, deren Ursprung in der Leber liegt. Das können Herz-Kreislauf-Erkrankungen sein, beispielsweise wenn das Protein, das die Forscher ausschalten wollen, in der Leber hergestellt wird.
Wenn die Forscher mit der RNA-Interferenz Krankheiten behandeln wollen, die ihren Ursprung zum Beispiel im Herzen oder im Gehirn haben, müssten sie ein anderes Transportmittel finden, um die siRNA in die Zellen einzuschleusen. Auch daran arbeitet Sanofi. Die Wissenschaftler suchen weitere Vehikel, um künftig auch andere Erkrankungen bekämpfen zu können.
Interdisziplinäres Team
Solch eine Vorgehensweise erfordert ein fachübergreifendes Team. So arbeiten bei Sanofi in Frankfurt Chemiker, Biologen, Pharmakologen und Mediziner gemeinsam an den Methoden: Die Chemiker stellen die siRNA-Teile her, die Biologen testen sie in der Zellkulturschale und die Pharmakologen und Mediziner überprüfen den Vorgang im Organismus.
Sanofi ist einer der Vorreiter dieser interdisziplinären Zusammenarbeit. Früher bestanden die Teams oft jeweils nur aus Wissenschaftlern einer Fachrichtung. Die RNA-Wissenschaftler haben früh erkannt, dass sie nur Erfolg haben können, wenn alle Experten eng zusammenarbeiten.
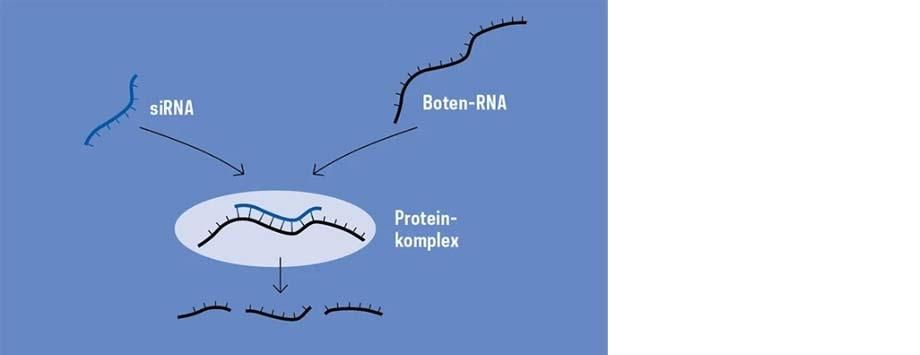
Die Boten-RNA wird ausgeschaltet, indem die so genannte „small interfering“ (siRNA) in die Zellen geschleust wird. Die siRNA wird in einen Proteinkomplex eingebaut. siRNA und Boten-RNA verbinden sich miteinander, die Boten-RNA wird zerschnitten und damit zerstört und das entsprechende Protein kann nicht mehr hergestellt werden.
Nobelpreis
Den Nobelpreis für Physiologie oder Medizin haben im Jahr 2006 die US-Wissenschaftler Andrew Z. Fire und Craig C. Mello erhalten – sie entdeckten den Mechanismus der RNA-Interferenz. Die RNA-Interferenz tritt bei Lebewesen auf und bestimmt zu einem ausschlaggebenden Teil, welche Gene aus der Masse der vorliegenden Erbinformationen tatsächlich genutzt werden. Frühere Konzepte gingen davon aus, dass Transkriptionsfaktoren dafür ausschlaggebend waren, ob eine Zelle ein bestimmtes Protein (und dementsprechend das Gen) auch tatsächlich braucht. Ende der 90er-Jahre wurde die RNA-Interferenz entdeckt – und damit wurde in diesem Zusammenhang auch der RNA eine größere Bedeutung zugesprochen.

Forschung & Entwicklung
Wir schaffen beste Bedingungen für biomedizinische Innovationen, um Krankheiten vorzubeugen, zu behandeln und zu heilen. Erfahren Sie mehr über unsere Aktivitäten im Bereich Forschung & Entwicklung.
Weitere Informationen
